FierceBiotech評(píng)選最具希望的十個(gè)晚期臨床候選藥
作者:呂順
FierceBiotech本周發(fā)布最具希望的十個(gè)晚期臨床候選藥。誠(chéng)然,“最具希望”藥物的評(píng)選有很大的主觀性,比如筆者就不完全同意這個(gè)結(jié)果,準(zhǔn)備在以后一段時(shí)間內(nèi)獨(dú)立評(píng)選,然后和Fierce Biotech的結(jié)果比對(duì)分析。以下是對(duì)這十個(gè)候選藥的簡(jiǎn)單介紹。
|
通用名
|
研發(fā)廠家
|
作用機(jī)理
|
三期臨床適應(yīng)癥
|
預(yù)計(jì)銷售峰值(億美元)
|
|
Sofosbuvir
|
Gilead
|
仿核苷酸藥
|
丙型肝炎
|
74
|
|
Nivolumab
|
施貴寶/小野制藥
|
PD-1抑制劑
|
實(shí)體瘤
|
60
|
|
Ibrutinib
|
強(qiáng)生/Pharmacyclics
|
BTK抑制劑
|
B細(xì)胞癌
|
60
|
|
MPDL3280A/RG7446
|
羅氏
|
PD-L1
|
實(shí)體瘤
|
30
|
|
VX-809/VX-661
|
Vertex
|
?
|
囊性纖維化
|
60
|
|
Lambrolizumab(MK-3475)
|
默克
|
PD-1抑制劑
|
實(shí)體瘤
|
30
|
|
Alirocumab
|
賽諾菲/ Regeneron
|
?PCSK9
|
降低低密度脂蛋白膽固醇(LDL)
|
30
|
|
ABT-450/r、ABT-267、ABT-333組合
|
AbbVie
|
?
|
丙型肝炎
|
30
|
|
Obinutuzumab/GA101
|
羅氏/ Biogen Idec
|
CD20
|
慢性淋巴細(xì)胞白血病
|
20
|
|
Dulaglutide
|
禮來(lái)
|
GLP-1抑制劑
|
糖尿病
|
17
|
1.Sofosbuvir:
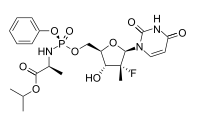
吉利德生物制藥公司的Sofosbuvir是一種仿核苷酸前藥(見(jiàn)上面結(jié)構(gòu)式),代謝后轉(zhuǎn)化為活性抗病毒劑2'-脫氧-2'-α-氟-β-C-甲基尿苷-5'-單磷酸酯。Sofosbuvir由Pharmasset發(fā)現(xiàn),Gilead Sciences收購(gòu)后開發(fā),目前處于III期臨床試驗(yàn)階段。吉利德的丙型肝炎藥物被認(rèn)為是眾多公司競(jìng)相開發(fā)的可免除干擾素使用的丙型肝炎藥物中最先進(jìn)的一個(gè)。今年二月份,吉利德宣布了sofosbuvir的兩項(xiàng)三期臨床實(shí)驗(yàn)結(jié)果,聲稱這兩項(xiàng)代號(hào)分別為Fission和Neutrino的臨床三期達(dá)到了預(yù)期療效指標(biāo)。臨床三期的Fission實(shí)驗(yàn)選擇感染2或3型丙肝病毒患者,隨機(jī)接受12周sofosbuvir與利巴韋林聯(lián)合用藥,或24周利巴韋林與聚乙二醇化干擾素聯(lián)合用藥(所謂標(biāo)準(zhǔn)療法)。治療結(jié)束時(shí)兩組病人都達(dá)到了67%的持久性病毒學(xué)應(yīng)答(SVR)。在Neutrino研究中,基因1型,4,5或6丙型肝炎病毒感染的患者進(jìn)行為期12周的sofosbuvir加利巴韋林與聚乙二醇化干擾素聯(lián)合用藥。治療結(jié)束病人都達(dá)到了90%(295/327)的持久性病毒學(xué)應(yīng)答(SVR)。而預(yù)期的只用利巴韋林與聚乙二醇化干擾素聯(lián)合用藥的SVR率為60%。在一項(xiàng)由美國(guó)國(guó)家衛(wèi)生研究院(NIH)組織的研究中sofosbuvir被證明甚至對(duì)于最棘手的丙型肝炎病例也是一種無(wú)干擾素的“安全和有效”治療途徑。今年八月,sofosbuvir被美國(guó)FDA認(rèn)定“突破性新藥”資格,預(yù)計(jì)年底能夠上市。Evaluate Pharma評(píng)估sofosbuvir的銷售峰值高達(dá)74億美元,遠(yuǎn)遠(yuǎn)高于其它機(jī)構(gòu)的估計(jì)數(shù)字。
2、Nivolumab:
程序性死亡蛋白-1(Programmed Death-1, PD-1)是一種跨膜蛋白,主要表達(dá)于活化的T細(xì)胞,屬CD28家族成員。盡管PD-1在1992年就被克隆,阻斷PD-1/B7H7通道的臨床意義直到2005年才被證實(shí),PD-1死亡通道是腫瘤細(xì)胞逃避免疫攻擊的重要途徑之一。為此,施貴寶、默克、羅氏等藥業(yè)巨頭制備了多種靶向PD-1的特異性單克隆抗體,而且顯示了初步抗腫瘤療效。
Nivolumab(也稱BMS-936558或ONO-4538或MDX1106)是施貴寶和Ono 制藥公司聯(lián)合研發(fā)的一種抗PD-1全人源IgG4單克隆抗體,目前處于III期臨床研究。在過(guò)去一年里,nivolumab一直是投資者關(guān)注的重點(diǎn),已經(jīng)在黑色素瘤、腎細(xì)胞癌和非小細(xì)胞肺癌等領(lǐng)域顯示良好的早期臨床結(jié)果。在今年的ASCO大會(huì)上,耶魯癌癥中心的Mario Sznol博士又報(bào)道了nivolumab的一項(xiàng)擴(kuò)展性實(shí)驗(yàn)。結(jié)果顯示:在采用nivolumab治療的107例轉(zhuǎn)移性黑色素瘤患者中,有33位患者的腫瘤縮小至少30%,另外還有11%的患者長(zhǎng)期保持病情穩(wěn)定,或者表現(xiàn)出非傳統(tǒng)的免疫相關(guān)應(yīng)答特征。經(jīng)過(guò)最長(zhǎng)時(shí)間達(dá)2年的隨訪,nivolumab在黑色素瘤患者中并未出現(xiàn)新的安全性問(wèn)題。接受nivolumab治療患者的中位總生存期接近17個(gè)月,2年生存率為43%。調(diào)整最佳劑量后(3毫克)總生存期可以達(dá)到20.3個(gè)月。盡管本次實(shí)驗(yàn)沒(méi)有對(duì)照組,但這個(gè)結(jié)果和威羅菲尼(Zelboraf)和伊匹單抗(Yervoy)過(guò)去的臨床結(jié)果相比有一定優(yōu)勢(shì)。這兩個(gè)藥的中位生存期分別為16和10個(gè)月,2年生存率為24%~33%。分析家預(yù)計(jì)nivolumab的銷售峰值在40至60億美元之間。
3、Ibrutinib (PCI-32765)
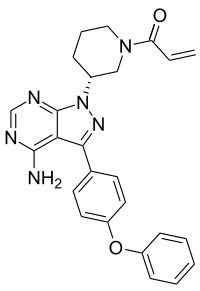
Ibrutinib(PCT-32765)是一種布魯頓酶(Bruton)酪氨酸激酶不可逆抑制劑,能有效地阻止腫瘤從B細(xì)胞遷移到適應(yīng)于腫瘤生長(zhǎng)環(huán)境的淋巴組織。據(jù)不完全統(tǒng)計(jì),ibrutinib已經(jīng)做過(guò)或者正在進(jìn)行23個(gè)臨床實(shí)驗(yàn),評(píng)價(jià)其單獨(dú)或聯(lián)合用藥,治療慢性淋巴細(xì)胞白血病(CLL)、復(fù)發(fā)/難治性套細(xì)胞淋巴瘤(MCL)、彌漫性大B細(xì)胞淋巴瘤、濾泡性淋巴瘤和多發(fā)性骨髓瘤。美國(guó)德克薩斯大學(xué)MD安德森癌癥中心的科學(xué)家在美國(guó)第54屆血液學(xué)協(xié)會(huì)年會(huì)上報(bào)道,Ibrutinib在一個(gè)二期臨床實(shí)驗(yàn)中治療復(fù)發(fā)/難治性套細(xì)胞淋巴瘤(mantle cell lymphoma)顯示良好療效。這個(gè)仍在進(jìn)行的二期臨床研究注冊(cè)有111位復(fù)發(fā)性/難治性套細(xì)胞淋巴瘤(MCL)患者,其中有或沒(méi)有使用bortezomib治療過(guò)的病人各占一半。結(jié)果發(fā)現(xiàn),有22%的病人呈現(xiàn)完全應(yīng)答,46%的患者部分應(yīng)答,總應(yīng)答率達(dá)68%,中位無(wú)進(jìn)展生存期13.9個(gè)月。這個(gè)實(shí)驗(yàn)結(jié)果和早期報(bào)道的初步結(jié)果一致。Ibrutinib由強(qiáng)生和Pharmacyclics聯(lián)合開發(fā),預(yù)計(jì)銷售峰值達(dá)60億美元。
4、MPDL 3280A(RG7446)
羅氏的MPDL3280A是一種工程化的抗體,靶向程序性死亡蛋白配體-1(PD-L1)蛋白。因?yàn)镻D-L1和PD-1的匙-鎖關(guān)系,靶向PD-L1和靶向PD-1能達(dá)到相同的分子生物學(xué)結(jié)果。也就是說(shuō),通過(guò)阻斷PD-L1和PD-1的結(jié)合,MPDL3280A能夠喚醒T細(xì)胞并識(shí)別癌細(xì)胞,通過(guò)持續(xù)生長(zhǎng)、增殖來(lái)更有效地攻擊癌細(xì)胞。目前,MPDL3280A正在進(jìn)行多個(gè)臨床實(shí)驗(yàn),用于治療晚期惡性黑色素瘤及其他實(shí)體瘤。因?yàn)镸PDL3280A不干擾PDL-2與PD1的結(jié)合,因此可能沒(méi)有肺炎等嚴(yán)重副反應(yīng)。依據(jù)公布的一個(gè)只含有30位患者的小型I期臨床數(shù)據(jù),每三周靜脈注射一次MPDL3280A治療的最大耐受劑量為20毫克/公斤。部分肺癌、腎癌、直腸癌和食道癌患者還顯示初步積極性療效。在最近舉行的2013年歐洲癌癥大會(huì)(ECC)上,羅氏披露了一項(xiàng)含有53例NSCLC患者的早期臨床實(shí)驗(yàn),尤其是針對(duì)吸煙的NSCLC患者,應(yīng)答率達(dá)到26%。羅氏/基因泰克的研究人員相信,采用抗 PDL-1單克隆抗體來(lái)靶向程序性死亡通道可能更安全,不會(huì)產(chǎn)生因靶向PD-1會(huì)同時(shí)下調(diào)PD-1—PDL-2的結(jié)合而引起的包括肺炎等副作用。盡管MPDL3280A還在早期臨床階段,分析家看好這款藥物,預(yù)計(jì)上市后銷售峰值達(dá)30億美元。
5. VX-809/VX-661
Vertex繼開發(fā)了抗丙肝藥物黃金標(biāo)準(zhǔn)Incivek以后,再次引起全球制藥業(yè)的關(guān)注,其囊性纖維化類藥的開發(fā)遙遙領(lǐng)先。Kalydeco(通用名:ivacaftor)榮膺美國(guó)FDA歷史上第一個(gè)“突破性新藥”稱號(hào)。福布斯分析家Matt Herper從基因?qū)W、發(fā)現(xiàn)過(guò)程和定價(jià)三個(gè)方面原因把Kalydeco列為2012年最重要新藥。藥源路人丙更闡述Kalydeco在多方面代表未來(lái)新藥的方向。今年早期,Vertex披露Kalydeco 和 VX-661 合用,顯著抑制F508del雙拷貝患者的cystic fibrosis肺部癥狀。VX-809和Kalydeco合用治療囊性纖維化CFTR基因F508del雙拷貝的病人也顯示積極療效。分析師預(yù)計(jì)VX-809/VX-661包括和Kalydeco聯(lián)合用藥,將會(huì)給Vertex帶來(lái)40至60億美元的收入。
6. Lambrolizumab(MK-3475):
Lambrolizumab是Merck開發(fā)的人源化抗PD-1單抗,目前處于II期臨床,用于治療晚期惡性黑色素瘤。Lambrolizumab在2013年4月被FDA授予突破性藥物資格。已公布的一個(gè)含有135個(gè)患者的Ib期臨床數(shù)據(jù)顯示,經(jīng)過(guò)每?jī)芍芤淮危看谓o藥10毫克/公斤的Lambrolizumab治療,52%的患者實(shí)現(xiàn)客觀抗腫瘤應(yīng)答,10%的患者實(shí)現(xiàn)完全應(yīng)答。對(duì)于之前已經(jīng)接受ipilimumab治療的患者,也有41%的患者實(shí)現(xiàn)客觀抗腫瘤應(yīng)答。目前,默克正在計(jì)劃一個(gè)不尋常的注冊(cè)患者多達(dá)1000人的一期臨床實(shí)驗(yàn),以期盡早取得lambrolizumab臨床申報(bào)所需的關(guān)鍵數(shù)據(jù)。Lambrolizumab將會(huì)是施貴寶nivolumab的強(qiáng)勁競(jìng)爭(zhēng)對(duì)手,Bernstein預(yù)計(jì)至2020年達(dá)到其銷售峰值30億美元。
7、Alirocumab
Alirocumab是靶向proprotein convertase subtilisin kexin 9(PCSK9)的一種全人源單克隆抗體,PCSK9和低密度脂蛋白膽固醇的表達(dá)密切相關(guān)。早在2006年,一項(xiàng)研究表明抑制PCSK9蛋白的表達(dá),能使低密度脂蛋白膽固醇的水平降低28%,使非洲美國(guó)人心血管病的風(fēng)險(xiǎn)降低88%。Alirocumab由Regeneron研制,和賽諾菲共同開發(fā),用于降低低密度脂蛋白膽固醇(LDL)。PCSK9抑制劑提供了一種新的治療模式,用來(lái)降低低密度脂蛋白膽固醇(LDL)的水平,被視為自Lipitor和Zocor等他汀類藥物之后,在對(duì)抗心臟疾病中所取得的最大進(jìn)步。一個(gè)alirocumab的三期臨床實(shí)驗(yàn)正在和默沙東的Zetia進(jìn)行頭對(duì)頭對(duì)比。之前雖然有數(shù)據(jù)證明alirocumab優(yōu)于Zetia,但該藥的最終成功,還依賴于涉及數(shù)千名患者的長(zhǎng)期研究,其中一些研究的數(shù)據(jù)將在5年后才能獲得。盡管如此,德意志銀行分析師預(yù)測(cè)alirocumab有望成為年銷售峰值超過(guò)30億美元的重磅炸彈型藥物。目前,安進(jìn)(Amgen)、輝瑞(Pfizer)、諾華(Novartis)和羅氏(Roche)等制藥巨頭也正密鑼緊鼓地推動(dòng)PCSK9抑制劑的開發(fā)。Alirocumab和安進(jìn)的AMG145處于領(lǐng)先地位。
9、Obinutuzumab(GA101,曾用名:afutuzumab)
Obibutuzumab是一種基因工程抗體,和美羅華一樣都靶向CD20。旨在使免疫系統(tǒng)更好地攻擊并殺死B細(xì)胞,尤其是通過(guò)基因改造之后和美羅華相比,對(duì)B細(xì)胞的攻擊效力更高。根據(jù)5月份披露的臨床數(shù)據(jù),羅氏的這款實(shí)驗(yàn)藥和瘤可寧(苯丁酸氮芥)聯(lián)合用藥時(shí),和單獨(dú)化療相比使病情進(jìn)展的風(fēng)險(xiǎn)降低86%,是化療治療的兩倍。該項(xiàng)臨床實(shí)驗(yàn)注冊(cè)有589名之前未曾接受過(guò)治療并伴有心臟疾病等其它健康問(wèn)題的慢性淋巴細(xì)胞性白血病(CLL)患者。聯(lián)合用藥組的總應(yīng)答率為75.5%,其中22%獲得安全應(yīng)答。相比之下,單獨(dú)用藥組的總應(yīng)答率只有30.2%,并且沒(méi)有患者表現(xiàn)完全應(yīng)答。無(wú)進(jìn)展生存期也由單獨(dú)用藥組的10.9個(gè)月延長(zhǎng)至23個(gè)月。與美羅華及單純化療相比,采用obibutuzumab治療的患者呈現(xiàn)嗜中性白血球減少癥,白細(xì)胞計(jì)數(shù)減少的發(fā)生率更高一些。今年七月,obinutuzumab被美國(guó)FDA授予“突破性藥物”稱號(hào)。innEvaluate Pharma預(yù)計(jì)obimutuzumab的銷售峰值在20億美元左右。
10、Dulaglutide
禮來(lái)的dulaglutide由GLP-1(7-37)通過(guò)連接一個(gè)IgG4的Fc單鏈以阻止二肽基肽酶4(DPP4)水解,是GLP-1受體激動(dòng)劑。從而增加餐后胰島素的釋放和減緩食物在胃腸道的吸收。今年6月,路透社報(bào)道dulaglutide每周注射給藥一次,可使血糖持續(xù)降低,比較服用二甲雙胍(metformin)、Byetta(exenatide injection,艾塞那肽注射液。在我國(guó)注冊(cè)名:百泌達(dá))和Januvia(Sitagliptin Phosphate Tablets,磷酸西格列汀片。在我國(guó)注冊(cè)名:捷諾維),它可以幫助更多患者血糖達(dá)到建議的控制目標(biāo)水平。目前還沒(méi)有發(fā)現(xiàn)有低血糖或嚴(yán)重低血糖病例報(bào)告。除此之外,該注射劑還能使患者的體重減輕,減輕的重量達(dá)到Januvia治療的兩倍,后者為默克公司創(chuàng)造40億美元年銷售額。
和比如二甲雙胍等口服藥物相比,該注射劑只需每周給藥一次。三項(xiàng)后期臨床結(jié)果表明, dulaglutide可能成為對(duì)付II型糖尿病的重要新武器。如果獲得批準(zhǔn),dulaglutide將與同樣是每周使用一次,施貴寶和阿斯利康的Bydureon(艾塞那肽緩釋注射用混懸液)和諾和諾德公司的Victoza(利拉魯肽注射液,諾和力)直接競(jìng)爭(zhēng)。初步數(shù)據(jù)顯示該藥和以上競(jìng)爭(zhēng)對(duì)手相比有一定優(yōu)勢(shì)。但在臨床試驗(yàn)中報(bào)道兩例胰腺癌病例,可能與Dulaglutide無(wú)關(guān)。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。
★更多深度解析訪問(wèn)《美中藥源》~
★ 請(qǐng)關(guān)注《美中藥源》微信公眾號(hào) ★

發(fā)表評(píng)論
要發(fā)表評(píng)論,您必須先登錄。


















 微信號(hào):美中藥源
微信號(hào):美中藥源